Las garrapatas han prosperado en las últimas décadas de forma alarmante gracias al cambio climático, ocasionando importantes pérdidas económicas y transmitiendo peligrosas enfermedades al hombre como la fiebre hemorrágica de Crimea-Congo, enfermedad de Lyme, encefalitis vírica, la anaplasmosis granulocítica humana y un largo etcétera. El cazador se encuentra en el centro de la diana del riesgo como colectivo.
¿QUÉ SON LAS GARRAPATAS?
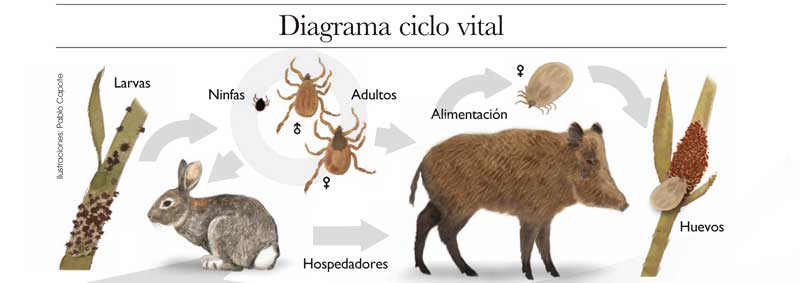
Las garrapatas son artrópodos que a lo largo de su ciclo de vida pasan por diferentes estados: huevo, larva, ninfa y adulto.
Se agrupan en dos grandes familias:
-Garrapatas blandas (argásidos), que son poco abundantes y presentan una cutícula externa flexible.
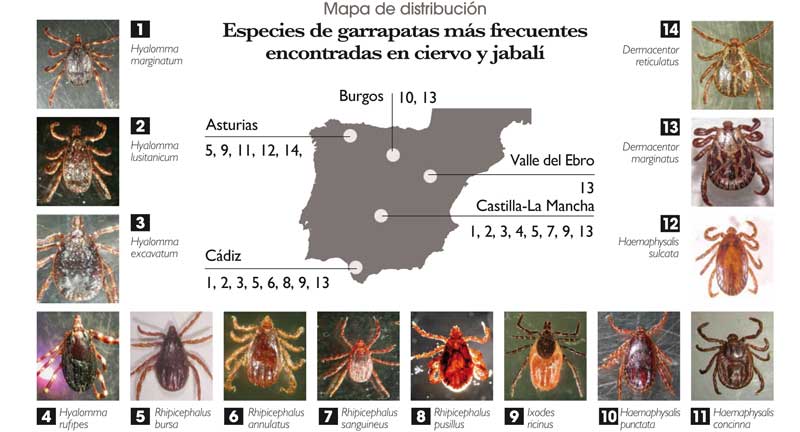
-Garrapatas duras (ixódidos), que poseen un escudo dorsal quitinoso y es la familia más numerosa y con mayor importancia médica y veterinaria.
Existe una tercera familia (Nuttalliellidae), compuesta por una única especie conocida.
Las garrapatas son ectoparásitos hematófagos obligados, es decir, que necesitan alimentarse de la sangre de sus hospedadores, proceso durante el cual pueden transmitir distintos patógenos que causan graves enfermedades.
La picadura de las garrapatas es normalmente indolora y se quedan fijadas a su hospedador firmemente, alimentándose durante largos periodos. Pueden parasitar a una gran variedad de especies animales en diferentes tipos de hábitats.
Su actividad tiene un importante carácter estacional, dependiendo de la temperatura y la humedad relativa principalmente, ya que son muy sensibles a la desecación, y la mayor parte de su vida la pasan fuera de su hospedador, refugiados en el suelo, en la vegetación o en las madrigueras o nidos de los hospedadores.
El impacto económico ocasionado por las garrapatas en el sector ganadero y cinegético, sectores de gran relevancia en España, es de gran importancia. Además, la máxima transcendencia de estos ectoparásitos es por ser vectores de agentes infecciosos (protozoos, virus, bacterias y hongos) para el ser humano y los animales.
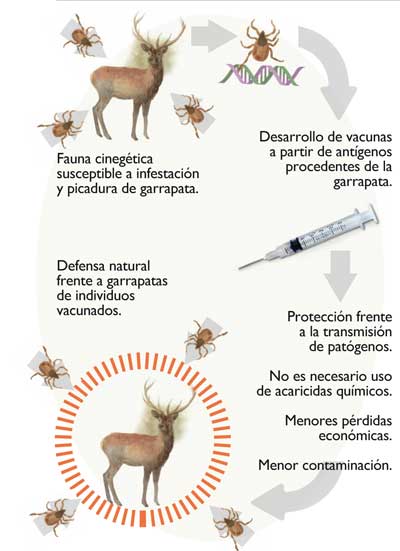
Los científicos de nuestro grupo de Sanidad y Biotecnología del Instituto de Investigación en Recursos Cinegéticos (IREC, CSIC-UCLM-JCCM), en colaboración con otras instituciones de dentro y fuera de España, han abordado esta problemática desde diversas perspectivas.
Gracias a estudios realizados por nuestro equipo, se ha detectado la existencia de determinados patógenos en garrapatas recogidas en Castilla-La Mancha, así como en otras regiones de España y del mundo. Por ejemplo, en 40 áreas de interés seleccionadas de CLM, el 18 % de las garrapatas capturadas resultaron infectadas con rickettsias, identificando mediante secuenciación especies pertenecientes al grupo de las fiebres manchadas, de gran interés por su patogenia en humanos.
Gracias a sus hospedadores, las garrapatas pueden diseminarse fácilmente debido a que permanecen fijadas sobre ellos durante un tiempo, por lo que pueden ser llevadas a distintos lugares por su hospedador.
Después de alimentarse durante varios días, se desprenden del hospedador y caen al suelo en un nuevo lugar; allí mudan y se reproducen, pudiendo alimentarse nuevamente sobre hospedadores de la zona y generar una nueva población de garrapatas; todo ello influiría en la dinámica de las enfermedades que transmiten y en el riesgo de incursión de patógenos nuevos en zonas en las que anteriormente no se encontraban, como podría ser el ejemplo de la fiebre hemorrágica de Crimea-Congo recientemente identificada en España por vez primera.
En general, el hombre es un hospedador accidental. Los humanos son infectados al entrar en zonas donde habitan las garrapatas y contactar con ellas. Además, la garrapata infectada no siempre transmite el patógeno, existiendo distintos factores que influyen en esta transmisión; por ejemplo, algunos patógenos requieren que la garrapata esté fijada más de un día a su hospedador para que se lleve a cabo dicha transmisión.






































Muy interesante la información, llevo batallando varias semanas con esta molesta plaga en mis perros. Me estaá funcionando muy bien el vinagre y los cítricos. Un saludo.